Aufbau der Materie
Entdecken Sie den faszinierenden mikroskopischen Aufbau unserer Welt! Alles, was wir sehen und berühren können, besteht aus unsichtbaren Teilchen, die auf faszinierende Weise angeordnet sind. Von den kleinsten Atomen bis zu komplexen Molekülen - verstehen Sie den Grundbaustein unseres Universums.
Lernziele
Nach diesem Themenbereich können Sie:
- Die Entwicklung der Atommodelle beschreiben
- Aufbau und Eigenschaften von Elementarteilchen erklären
- Das Periodensystem der Elemente lesen und interpretieren
- Verschiedene chemische Bindungen unterscheiden
- Die Bedeutung von Ionen für die Stoffeigenschaften verstehen
Was ist Materie?
Materie ist alles, was Masse und Volumen besitzt. Sie besteht aus kleinsten Teilchen, den Atomen. Atome können allein oder in Verbindung mit anderen Atomen Moleküle bilden.
Die Aggregatzustände der Materie
| Aggregatzustand | Anordnung der Teilchen | Bewegung | Beispiel |
|---|---|---|---|
| fest | Regelmäßig, dicht gepackt | Schwingen am Platz | Eis, Eisen |
| flüssig | Unregelmäßig, nah beieinander | Bewegen sich aneinander | Wasser, Quecksilber |
| gasförmig | Große Abstände, regellos | Schnell, frei beweglich | Sauerstoff, Wasserdampf |
Die Elementarteilchen des Atoms
Atome bestehen aus drei wichtigsten Teilchen:
1. Protonen (p⁺)
- Ladung: +1 Elementarladung
- Masse: 1.0073 u (atomare Masseneinheit)
- Ort: Im Atomkern
- Anzahl: Bestimmt das Element (Ordnungszahl)
2. Neutronen (n⁰)
- Ladung: Neutral (keine Ladung)
- Masse: 1.0087 u
- Ort: Im Atomkern
- Anzahl: Variiert (Isotope)
3. Elektronen (e⁻)
- Ladung: -1 Elementarladung
- Masse: 0.00055 u (sehr leicht)
- Ort: In der Elektronenhülle um den Kern
- Anzahl: Gleich der Protonenzahl (bei neutralen Atomen)
Struktur des Atoms
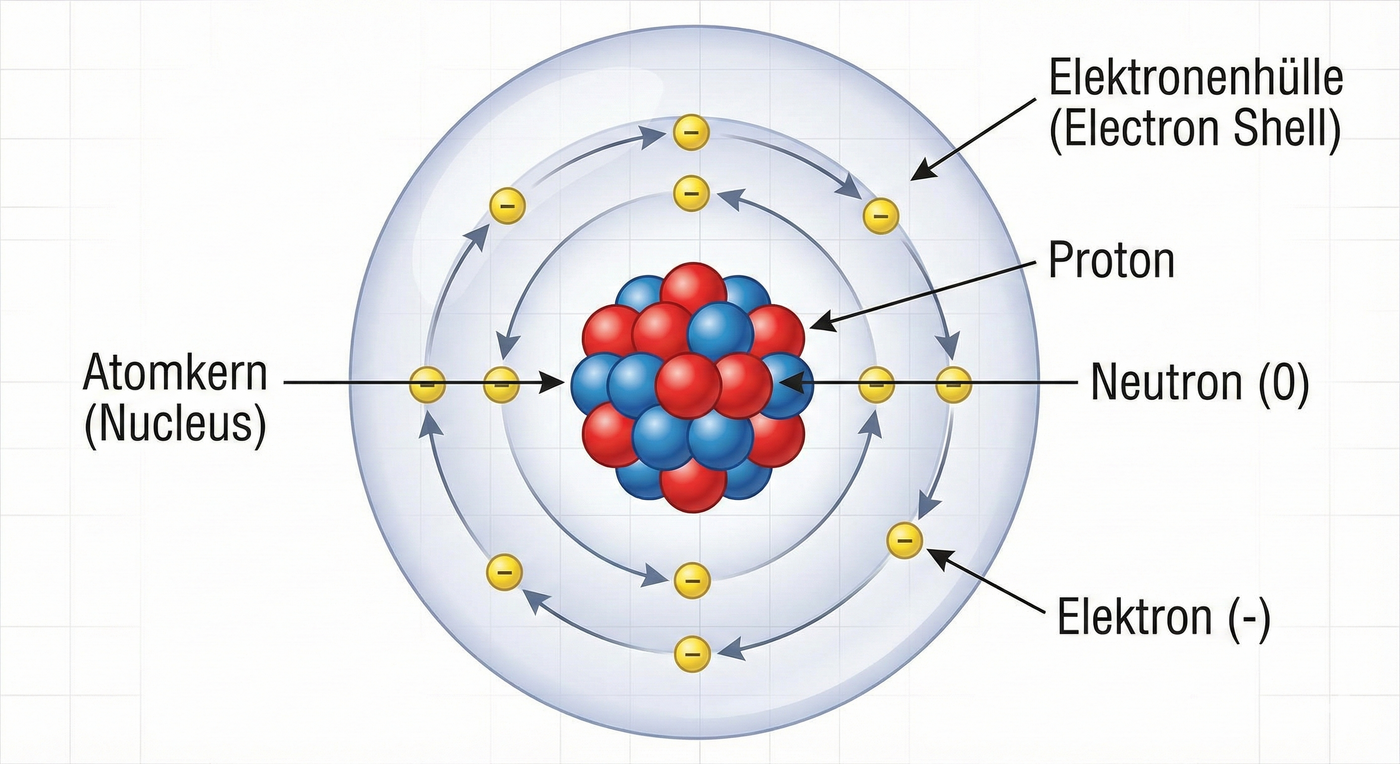
Das Atom besteht aus einem kompakten Kern mit Protonen und Neutronen, umgeben von einer Elektronenhülle.
Wichtige Größen:
- Protonenzahl (Z): Anzahl der Protonen = Ordnungszahl
- Massenzahl (A): Protonen + Neutronen
- Elektronenzahl: Bei neutralen Atomen = Protonenzahl
Beispiel: Kohlenstoff-12 (¹²C)
- Protonenzahl Z = 6
- Neutronenzahl N = 6
- Massenzahl A = 12
- Elektronenzahl = 6
Die Entwicklung der Atommodelle
1. Daltons Atommodell (1803)
John Dalton stellte die Atomhypothese auf:
- Materie besteht aus unteilbaren Teilchen (Atomen)
- Atome eines Elements sind identisch
- Atome verschiedener Elemente haben unterschiedliche Massen
- Atome können sich verbinden, aber nicht verändert werden
2. Thomsons Atommodell (1904) - “Rosinenkuchenmodell”
J.J. Thomson entdeckte das Elektron:
- Positive Masse gleichmäßig verteilt (“Kuchenteig”)
- Negative Elektronen eingebettet (“Rosinen”)
- Atom ist elektrisch neutral
3. Rutherfords Atommodell (1911) - “Kern-Hülle-Modell”
Ernest Rutherford führte das berühmte Streuexperiment durch:
- Positiver Kern im Zentrum (winzig, aber schwer)
- Große leere Hülle mit Elektronen
- Vergleich: Wie eine Fliege (Elektron) in einer Kathedrale (Atom)
4. Bohrsches Atommodell (1913)
Niels Bohr erweiterte das Modell:
- Elektronen bewegen sich auf definierten Bahnen (Schalen)
- Jede Schale hat eine bestimmte Energie
- Elektronen können zwischen Schalen springen (Energieabgabe/ -aufnahme)
Bohrsche Postulate:
- Elektronen kreisen auf diskreten Bahnen um den Kern
- Auf diesen Bahnen strahlen sie keine Energie ab
- Energie wird nur bei Quantensprüngen abgegeben/absorbiert
5. Orbitalmodell (heute gültig)
Das moderne quantenmechanische Modell:
- Keine genauen Bahnen, sondern Orbitale (Aufenthaltswahrscheinlichkeiten)
- Elektronenwolke um den Kern
- Vier Quantenzahlen beschreiben den Zustand eines Elektrons
Das Periodensystem der Elemente
Aufbau des Periodensystems
Das Periodensystem ordnet alle 118 bekannten Elemente nach:
- Ordnungszahl (Protonenzahl) - von oben nach unten
- Ähnlichen Eigenschaften - in Gruppen (senkrecht)
Struktur
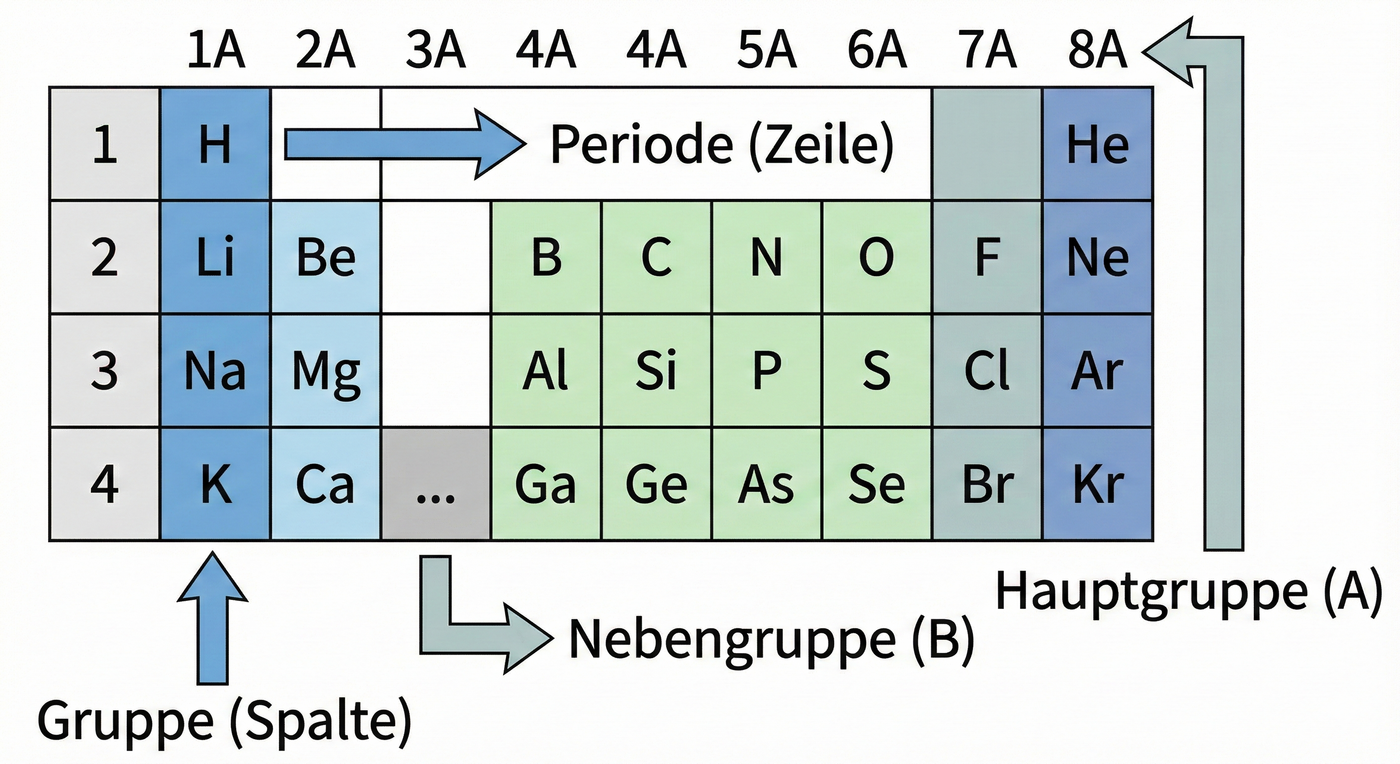
Legende:
- Hauptgruppe (A): Gruppen 1-2 und 13-18
- Nebengruppe (B): Gruppen 3-12 (Übergangsmetalle)
- Periode: Zeilen (1-7)
- Gruppe: Spalten
Wichtige Gruppen
Hauptgruppen (1-2, 13-18):
- Alkalimetalle (1): Li, Na, K, Rb, Cs, Fr - sehr reaktiv
- Erdalkalimetalle (2): Be, Mg, Ca, Sr, Ba, Ra - reaktiv
- Halogene (17): F, Cl, Br, I, At - sehr reaktiv, nichtmetalle
- Edelgase (18): He, Ne, Ar, Kr, Xe, Rn - sehr reaktionsträge
Nebengruppen (3-12): Übergangsmetalle (z.B. Fe, Cu, Zn, Au)
Perioden (Zeilen)
- Periode 1: 2 Elemente (H, He)
- Periode 2+3: 8 Elemente
- Periode 4+5: 18 Elemente
- Periode 6+7: 32 Elemente (inkl. Lanthanoide/Actinoide)
Informationen im Periodensystem
Für jedes Element können Sie ablesen:
- Ordnungszahl: Anzahl der Protonen
- Symbol: Abkürzung (z.B. C für Kohlenstoff)
- Atommasse: Durchschnittsmasse aller Isotope
- Elektronenkonfiguration: Verteilung der Elektronen
🧪 Interaktiv: Erkunden Sie das Periodensystem 3D und erfahren Sie mehr über jedes Element!
Chemische Bindungen
Ionenbindung (Elektrovalenz)
Bei der Ionenbindung werden Elektronen vollständig übertragen.
Vorgang:
- Metall gibt Elektronen ab → Kation (positiv geladen)
- Nichtmetall nimmt Elektronen auf → Anion (negativ geladen)
- Elektrostatische Anziehung zwischen Ionen
Beispiel: Natriumchlorid (Kochsalz)
$$\ce{Na -> Na+ + e-} \quad \text{(Natrium gibt 1 Elektron ab)}$$
$$\ce{Cl + e- -> Cl-} \quad \text{(Chlor nimmt 1 Elektron auf)}$$
$$\ce{Na+ + Cl- -> NaCl} \quad \text{(Ionenbindung)}$$
Eigenschaften ionischer Verbindungen:
- Hoher Schmelzpunkt (> 300°C)
- Hart und spröde
- Leiten Strom als Schmelze oder Lösung
- Kristalline Struktur
Beispiele: NaCl, MgO, CaF₂
Atombindung (Kovalente Bindung)
Bei der Atombindung werden Elektronen gemeinsam verwendet.
Vorgang:
- Beide Atome stellen Elektronen zur Verfügung
- Ein Elektronenpaar wird geteilt (bindend)
- Jedes Atom erreicht stabile Elektronenkonfiguration
Beispiel: Wasser ($\ce{H2O}$)
$$\ce{H. + .O. + .H -> H-O-H} \quad \text{(8 } e^- \text{)}$$
Arten der Atombindung:
- Einfachbindung: 1 Elektronenpaar (z.B. H-H, H-Cl)
- Doppelbindung: 2 Elektronenpaare (z.B. O=O, C=O)
- Dreifachbindung: 3 Elektronenpaare (z.B. N≡N, C≡C)
Eigenschaften kovalenter Verbindungen:
- Niedriger Schmelzpunkt (< 300°C)
- Oft flüssig oder gasförmig bei Raumtemperatur
- Leiten keinen Strom
- Molekulare Struktur
Beispiele: H₂O, CO₂, CH₄, O₂
Metallische Bindung
Bei Metallen sind die Atome durch “Elektronengas” verbunden.
Vorgang:
- Metallatome geben Elektronen ab
- Elektronen bewegen sich frei zwischen allen Kationen
- Anziehung zwischen Elektronengas und Metallkationen
Eigenschaften:
- Gute elektrische Leitfähigkeit
- Gute Wärmeleitfähigkeit
- Verformbar (duktil)
- Metallischer Glanz
Beispiele: Fe, Cu, Ag, Au, Al
Van-der-Waals-Kräfte
Schwache Anziehungskräfte zwischen Molekülen:
- Dipol-Dipol-Kräfte: Zwischen polaren Molekülen
- London-Kräfte: Zwischen allen Molekülen (temporäre Dipole)
Ionen und ihre Bedeutung
Was sind Ionen?
Ionen sind geladene Teilchen:
- Kationen: Positiv geladen (weniger Elektronen als Protonen)
- Anionen: Negativ geladen (mehr Elektronen als Protonen)
Bildung von Ionen
Metalle geben Elektronen ab → Kationen:
- $\ce{Na -> Na+ + e-}$
- $\ce{Mg -> Mg^2+ + 2e-}$
Nichtmetalle nehmen Elektronen auf → Anionen:
- $\ce{Cl + e- -> Cl-}$
- $\ce{O + 2e- -> O^2-}$
Wichtige Ionen im Alltag
| Kation | Name | Anion | Name |
|---|---|---|---|
| Na⁺ | Natrium | Cl⁻ | Chlorid |
| K⁺ | Kalium | Br⁻ | Bromid |
| Ca²⁺ | Calcium | O²⁻ | Oxid |
| Mg²⁺ | Magnesium | OH⁻ | Hydroxid |
| Fe²⁺ | Eisen(II) | SO₄²⁻ | Sulfat |
| Fe³⁺ | Eisen(III) | CO₃²⁻ | Carbonat |
Bedeutung von Ionen
Biologische Systeme:
- Natrium/Kalium für Nervenimpulse
- Calcium für Knochen und Zellfunktion
- Chlorid für Verdauung
Technische Anwendungen:
- Batterien und Akkus
- Galvanische Elemente
- Elektrolyse
Isotope
Isotope sind Atome desselben Elements mit unterschiedlicher Neutronenzahl.
Beispiel: Kohlenstoff-Isotope
- ¹²C: 6 Protonen, 6 Neutronen (98.9%)
- ¹³C: 6 Protonen, 7 Neutronen (1.1%)
- ¹⁴C: 6 Protonen, 8 Neutronen (radioaktiv, für Altersbestimmung)
Praktische Anwendungen
Experiment: Wasserstoff-Eigenherstellung
Material:
- Zink
- Salzsäure (verdünnt)
- Reagenzglas
- Stöpsel mit Ableitungsrohr
- Glimmspan
Durchführung:
- Zink in Reagenzglas geben
- Salzsäure hinzufügen
- Glimmspan an das Ableitungsrohr halten
- Knallprobe machen
Ergebnis: $$\ce{Zn + 2HCl -> ZnCl2 + H2}$$
- Gasentwicklung: Wasserstoff
- Knall bei der Knallprobe
VR-Erfahrung: Atombau erleben
🕶️ PSE in VR - Tauchen Sie virtuell in die Welt der Atome ein!
Zusammenfassung
- Atome bestehen aus Protonen, Neutronen und Elektronen
- Protonenzahl bestimmt das Element, Massenzahl = Protonen + Neutronen
- Atommodelle entwickelten sich von Dalton über Bohr zum Orbitalmodell
- Periodensystem ordnet Elemente nach Ordnungszahl und Eigenschaften
- Ionenbindung: Elektronenübertragung (Metall + Nichtmetall)
- Atombindung: Elektronenpaar-Bildung (Nichtmetall + Nichtmetall)
- Metallische Bindung: Elektronengas zwischen Metallkationen
- Ionen sind geladene Teilchen (Kationen +, Anionen -)
Weiterführende Themen
- Quantenzahlen und Orbitale
- Hybridisierung der Orbitale
- Molekülgeometrie (VSEPR-Modell)
- Kristallstrukturen
- Metallurgie und Legierungen
Interaktive Tools
⚛️ Periodensystem 3D - Interaktives 3D-Periodensystem mit detaillierten Informationen zu allen 118 Elementen
🕶️ VR Atombau - Erleben Sie den Aufbau von Atomen in Virtual Reality
Testen Sie Ihr Wissen
- Wie viele Protonen hat ein Sauerstoff-Atom?
- Was ist der Unterschied zwischen einer Ionenbindung und einer Atombindung?
- Welches Element hat die Ordnungszahl 6?
Erstellt: 27. Dezember 2025 Themenbereich: Aufbau der Materie Schwierigkeit: Grundlagen
 chemie-lernen.org - 📖 Offene, 🖱️ Interaktive und 🥽 Immersive Lerninhalte
chemie-lernen.org - 📖 Offene, 🖱️ Interaktive und 🥽 Immersive Lerninhalte